entsyymit
määritelmä
Entsyymit ovat kemiallisia aineita, joita löytyy kehosta. He asettavat kehossa kemiallisia reaktioita.
historia
Sana entsyymi oli kotoisin Wilhelm Friedrich Kühne 1878 ja on johdettu kreikkalaisesta sanasta Enzmon, joka tarkoittaa hiivaa tai hapanta. Sitten se löysi tien kansainväliseen tieteeseen. puhtaan sovelletun kemian kansainvälinen liitto (IUPAC) ja biokemian kansainvälinen liitto (IUBMB) laati entsyymien nimikkeistön, joka määrittelee tämän suuren aineryhmän edustajat yhdeksi ryhmäksi. Nimeäminen, joka luokittelee entsyymit niiden tehtävien mukaan, on tärkeä yksittäisten entsyymien tehtävien määrittämisessä.
Kuva entsyymeistä
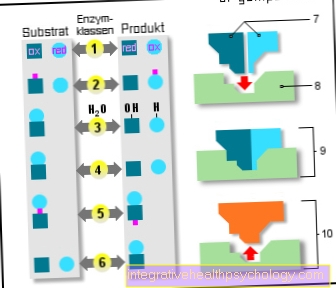
entsyymit
6 entsyymiluokkaa:
- oksidoreduktaasit
(Hapetus / pelkistys) - transferaasit
(Tarttuminen) - hydrolaasit
(Veden käyttö) - lyaasit
(Pilkkominen) - isomeraaseihin
(sama molekyylikaava) - ligaaseista
(Lisäysreaktiot) - substraatit
- Aktiivinen keskus
- Entsyymi / substraatti
monimutkainen - Entsyymi / tuote
monimutkainen
Katsaus kaikkeenDr-Gumpertin kuvat löytyvät osoitteesta: lääketieteelliset piirrokset
nimeäminen
nimeäminen entsyymi on päällä kolme perusperiaatetta perustuu.Entsyymien nimet, jotka päättyvät inaasiin, kuvaavat useita entsyymejä järjestelmässä. Entsyyminimi itse kuvaa reaktiota, jonka entsyymi liikkuu (katalysoitua). Entsyyminimi on myös entsyymin luokittelu. Lisäksi koodijärjestelmä, joka EY-numerojärjestelmä, jossa entsyymit valmistetaan numerokoodilla neljä numeroa voidaan löytää. Ensimmäinen numero osoittaa entsyymiluokan. Kaikkien havaittujen entsyymien luettelot varmistavat, että määritelty entsyymikoodi löytyy nopeammin. Vaikka koodit perustuvat entsyymin katalysoiman reaktion ominaisuuksiin, käytännössä numeeriset koodit osoittautuvat hankaliksi. Yllä oleviin sääntöihin perustuvia systemaattisia nimiä käytetään useammin. Nimikkeistöön liittyy ongelmia esimerkiksi entsyymien kanssa, jotka katalysoivat useita reaktioita. Siksi heillä on joskus useita nimiä. Joillakin entsyymeillä on triviaalia nimeä, jotka eivät tarkoita, että mainittu aine on entsyymi. Koska nimiä käytettiin perinteisesti laajalti, osa niistä säilytettiin.
Luokittelu entsyymifunktion mukaan
IUPAC: n ja IUBMB: n mukaan entsyymit jaetaan kuuteen entsyymiluokkaan niiden käynnistämän reaktion mukaan:
- oksidoreduktaasit
Oksidoreduktaasit käynnistivät redox-reaktiot. Tässä kemiallisessa reaktiossa elektronit kulkevat reaktiopartnerista toiseen. Yhdestä aineesta vapautuu elektroneja (hapettuminen) ja toiseen aineeseen otetaan elektroneja (pelkistys).
Kaava katalysoidulle reaktiolle on A + + APa + +.
Aine A vapauttaa elektronin (?) Ja hapetetaan, kun taas aine B absorboi tämän elektronin ja pelkistyy. Siksi redox-reaktioita kutsutaan myös pelkistys-hapettumisreaktioiksi.
Monet metaboliset reaktiot ovat redox-reaktioita. Hapegenaasit siirtyvät substraattiinsa yhden tai useamman happiatomin. - transferaasit
Transferaasit siirtävät funktionaalisen ryhmän substraatista toiseen. Funktionaaliset ryhmät ovat orgaanisten yhdisteiden atomiryhmiä, jotka määräävät aineen ominaisuudet ja reaktiokäyttäytymisen suuressa määrin. Kemialliset yhdisteet, joilla on samat funktionaaliset ryhmät, on ryhmitelty aineluokkiin niiden samanlaisten ominaisuuksien vuoksi. Funktionaaliset ryhmät jaetaan sen mukaan, ovatko heteroatomit vai eivät. Heteroatomit ovat kaikki orgaanisten yhdisteiden atomeja, jotka eivät ole hiiltä eikä vetyä.
Esimerkiksi: -OH -> hydroksyyliryhmä (alkoholit) - hydrolaasit
Hydrolaasit jakavat sidokset palautuviin reaktioihin vettä käyttämällä. Esterit, esterit, peptidit, glykosidit, happoanhydridit tai C-C-sidokset. Tasapainoreaktio on: A-B + H20? A-H + B-OH.
Hydrolaasien ryhmään kuuluva entsyymi on esim. Alfa-galaktosidaasi. - lyaasit
Lysaasit, joita kutsutaan myös synteesiksi, katalysoivat monimutkaisten tuotteiden pilkkoutumista yksinkertaisista substraateista jakamatta ATP: tä. Reaktiokaavio on A-B → A + B.
ATP on adenosiinitrifosfaatti ja nukleotidi, joka koostuu nukleosidi-adenosiinin trifosfaatista (ja sellaisena nukleiinihappo RNA: n energiarikas rakennuspalikka). ATP on kuitenkin pääasiassa jokaisessa solussa välittömästi saatavilla olevan energian universaali muoto ja samalla tärkeä energiantoimitusprosessien säätelijä. Tarvittaessa ATP syntetisoidaan uudelleen muista energiavarastoista (kreatiinifosfaatti, glykogeeni, rasvahapot). ATP-molekyyli koostuu adeniinitähteestä, sokeririboosista ja kolmesta fosfaatista (a To?) Esterissä (a) tai anhydridisidoksista (a ja a). - isomeraaseihin
Isomeraasit nopeuttavat isomeerien kemiallista muuntamista. Isomerismi on kahden tai useamman kemiallisen yhdisteen esiintyminen, joilla on täsmälleen samat atomit (sama empiirinen kaava) ja molekyylipainot, jotka kuitenkin eroavat toistensa yhteydessä tai atomien alueellisessa järjestelyssä. Vastaavia yhdisteitä kutsutaan isomeereiksi.
Nämä isomeerit eroavat kemiallisista tai fysikaalisista ja usein myös biokemiallisista ominaisuuksistaan. Isomerismia esiintyy pääasiassa orgaanisten yhdisteiden, mutta myös (epäorgaanisten) koordinaatioyhdisteiden kanssa. Isomerismi on jaettu eri alueisiin. - ligaaseista
Ligaasit katalysoivat sellaisten aineiden muodostumista, jotka ovat kemiallisesti monimutkaisempia kuin käytetyt substraatit, mutta toisin kuin lyaasit, ovat vain entsymaattisesti tehokkaita ATP: n pilkkomisella. Näiden aineiden muodostuminen vaatii siis energiaa, joka saadaan jakamalla ATP.
Jotkut entsyymit kykenevät katalysoimaan useita, joskus hyvin erilaisia reaktioita. Jos näin on, ne osoitetaan useisiin entsyymiluokkiin.
Saatat olla kiinnostunut myös näistä artikkeleista:
- Alfa-glukosidaasi
- lipaasi
- trypsiini
Luokittelu entsyymirakenteen mukaan
Lähes kaikki entsyymit ovat proteiineja, ja ne voidaan luokitella proteiiniketjun pituuden mukaan:
- monomeerit
Entsyymit, jotka koostuvat vain yhdestä proteiiniketjusta - oligomeerit
Entsyymit, jotka koostuvat useista proteiiniketjuista (monomeereistä) - Monentsyymiketjut
Useita aggregoituneita entsyymejä, jotka toimivat yhdessä ja säätelevät toisiaan. Nämä entsyymiketjut katalysoivat peräkkäisiä vaiheita solun aineenvaihdunnassa.
Lisäksi on olemassa yksittäisiä proteiiniketjuja, jotka sisältävät useita entsyymiaktiivisuuksia; näitä kutsutaan monitoiminnallisiksi entsyymeiksi.
Luokittelu kofaktorien mukaan
Toinen luokittelu on luokittelu kofaktorien huomion perusteella. Kofaktorit, koentsyymit ja lisäsubstraatit ovat eri aineiden luokituksia, jotka vaikuttavat biokemiallisiin reaktioihin vuorovaikutuksessaan entsyymien kanssa.
Orgaanisia molekyylejä ja ioneja (lähinnä metalli-ioneja) pidetään.
Puhtaat proteiinientsyymit koostuvat yksinomaan proteiineista ja aktiivinen keskus muodostuu vain aminohappotähteistä ja peptidin runko-osasta. Aminohapot ovat orgaanisten yhdisteiden luokka, joissa on ainakin yksi karboksiryhmä (-COOH) ja yksi aminoryhmä (-NH2).
Holoentsyymit koostuvat proteiinikomponentista, apoentsyymistä ja kofaktorista, pienimolekyylipainoisesta molekyylistä (ei proteiinista). Molemmat yhdessä ovat tärkeitä entsyymin toiminnalle.
coenzymes
Kofaktoreina olevia orgaanisia molekyylejä kutsutaan koentsyymeiksi. Jos ne sitoutuvat kovalenttisesti apoentsyymiin, niitä kutsutaan proteesiryhmiksi tai lisäsubstraateiksi. Proteesiryhmä on termi, jota käytetään kuvaamaan ei-proteiinikomponentteja, jotka ovat sitoutuneet tiukasti (yleensä kovalenttisesti) proteiiniin, jolla on katalyyttinen vaikutus.
Kosubstraatit ovat nimiä erilaisille luokituksille aineille, jotka vaikuttavat biokemiallisiin reaktioihin vuorovaikutuksessaan entsyymien kanssa. Biokatalyytteinä molekyylit kiihdyttävät reaktioita organismeissa, entsyymit kiihdyttävät biokemiallisia reaktioita. Ne vähentävät aktivointienergiaa, joka on ylitettävä, jotta aine voidaan muuttaa.